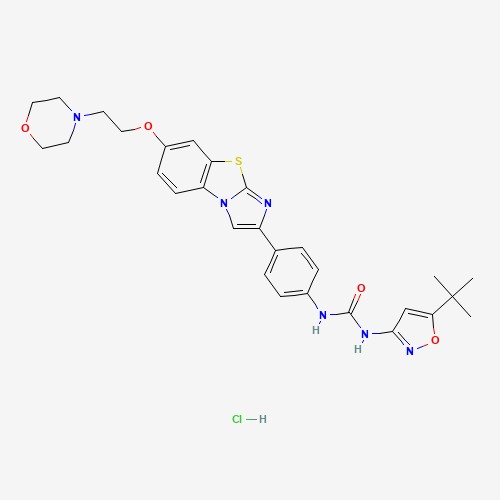
성분 상세정보
정보 수정요청| 성분명 | 퀴자티닙염산염 (Quizartinib hydrochloride) |
분자식 : C29H33ClN6O4S 분자량 : 597.1g/mol PubChem CID 25235536 |
|---|---|---|
| 동의어 |
|
|
| 작용기전 | 퀴자르티닙은 FDA 승인 검사에서 FLT3 내부 반복 이중복제(ITD) 양성으로 확인된 새로 진단된 성인 급성 골수성 백혈병(AML) 환자의 치료를 위해 표준 시타라빈 및 안트라사이클린 유도 요법 및 시타라빈 강화 요법과 병용하여, 그리고 강화 화학 요법 후 유지 단독 요법으로 사용됩니다.
출처: DrugBank 'Quizartinib' https://go.drugbank.com/drugs/DB12874 (Accessed 26.01.27) |
|
| 약동학 | (1) 흡수
정제 제형에서 퀴자티닙의 절대 생체이용률은 71 %였다. 건강한 성인에게 공복 상태에서 경구 투여 시 퀴자티닙 및 AC886의 최고 농도 도달 시간(Tmax 중앙값)은 각각 약 4시간(범위 2 - 8시간) 및 5 - 6시간(범위 4 - 120시간)이었다. 53 mg/일 용량으로 유지요법 중 정상 상태에서, 퀴자티닙 및 AC886의 기하평균(%CV) Cmax는 각각 529 ng/mL(60 %) 및 262 ng/mL(48 %)로 추정되었고, 기하평균(%CV) AUC0-24h는 각각 10,200 ng·h/mL(75 %) 및 5,790 ng·h/mL(46 %)였다. 음식과 함께 이 약 투여 시 퀴자티닙 Cmax는 8% 감소하였으며, AUCinf는 8% 증가하였다. Tmax는 2시간 지연되었다. 이 약은 음식 여부와 관계없이 투여 가능하다. (2) 분포 퀴자티닙 및 AC886의 In vitro 사람 혈장 단백질 결합률은 각각 99% 이상이다. 10 - 1,000 ng/mL 농도 범위에서 in vitro 적혈구 내 퀴자티닙 및 AC886의 혈액 대 혈장 비율은 각각 0.79 - 1.30 및 1.36 - 3.19이다. 건강한 성인에서 퀴자티닙의 정상 상태에서 분포 용적(Vss)의 기하평균(%CV)은 275 L(17%)로 추정되었다. (3) 생체 내 변환 퀴자티닙은 활성 대사체 AC886을 생성하는 산화 경로를 통해 in vitro에서 CYP3A4/5에 의해 주로 대사되며, 이후 CYP3A4/5에 의해 추가로 대사된다. 유지요법 중 정상 상태에서 퀴자티닙에 대한 AC886의 AUC0-24h비는 0.57이었다. (4) 배설 퀴자티닙 및 AC886의 유효 반감기(t1/2)의 평균(표준편차)는 새로 진단된 급성 골수성 백혈병 환자에서 각각 81시간(±73) 및 136시간(±113)이다. 퀴자티닙 및 AC886의 축적비의 평균 AUC0-24h(표준편차)는 각각 5.4(±4.4) 및 8.7(±6.8)이었다. 퀴자티닙 및 그 대사체는 대부분이 일차적으로 간담도 경로를 통해 제거되어 대변으로 배설된다(경구 투여된 방사성 동위원소 표지 투여량의 76.3 %). 대변으로 배설되는 미변화체 퀴자티닙은 경구 투여된 방사성 동위원소 표지 투여량의 약 4 %였다. 신배설은 투여된 방사성 동위원소 표지량 제거의 부수적 경로이다(2 % 미만). 건강한 성인에서 퀴자티닙의 기하평균(%CV) 전신 청소율(CL)은 2.23 L/hour(29%)로 추정되었다. 출처: 식품의약품안전처 '반플리타정' 의약품상세정보 https://nedrug.mfds.go.kr/pbp/CCBBB01/getItemDetailCache?cacheSeq=202600219aupdateTs2026-01-26%2018:28:58.986969b (Accessed 26.01.27) |
※ 이상반응, 금기, 주의사항, 상호작용 등의 정보는 개별 의약품의 허가정보에서 확인하실 수 있습니다.